2025-06-18
有临来雅

在传统的I/II期肿瘤临床研究中,常基于毒性和疗效随剂量递增而单调增加的假设,寻找最大耐受剂量(MTD)和II期推荐剂量(RP2D)。但对于靶向药物和免疫疗法,剂量的增加并不意味着疗效的提高。此时需要用到最优生物剂量(如OBD),该剂量可能低于MTD,基于效用的模型辅助设计U-BOIN(Utility-based Bayesian Optimal Interval)设计恰恰可以寻找OBD。U-BOIN设计优势如下:
一、U-BOIN设计思路
U-BOIN是一种基于多项式-狄利克雷模型的 I/II 期设计方法,对毒性和疗效进行建模,并采用效用函数来衡量剂量风险-收益的权衡。该设计由两个无缝阶段组成,流程图见图 1。
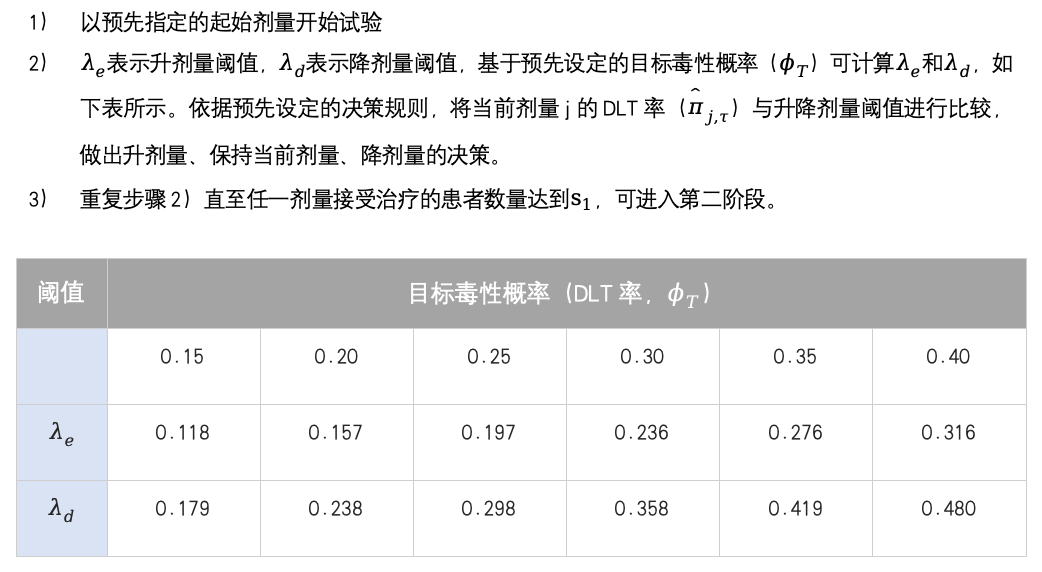
表1:BOIN 设计的剂量升降阈值
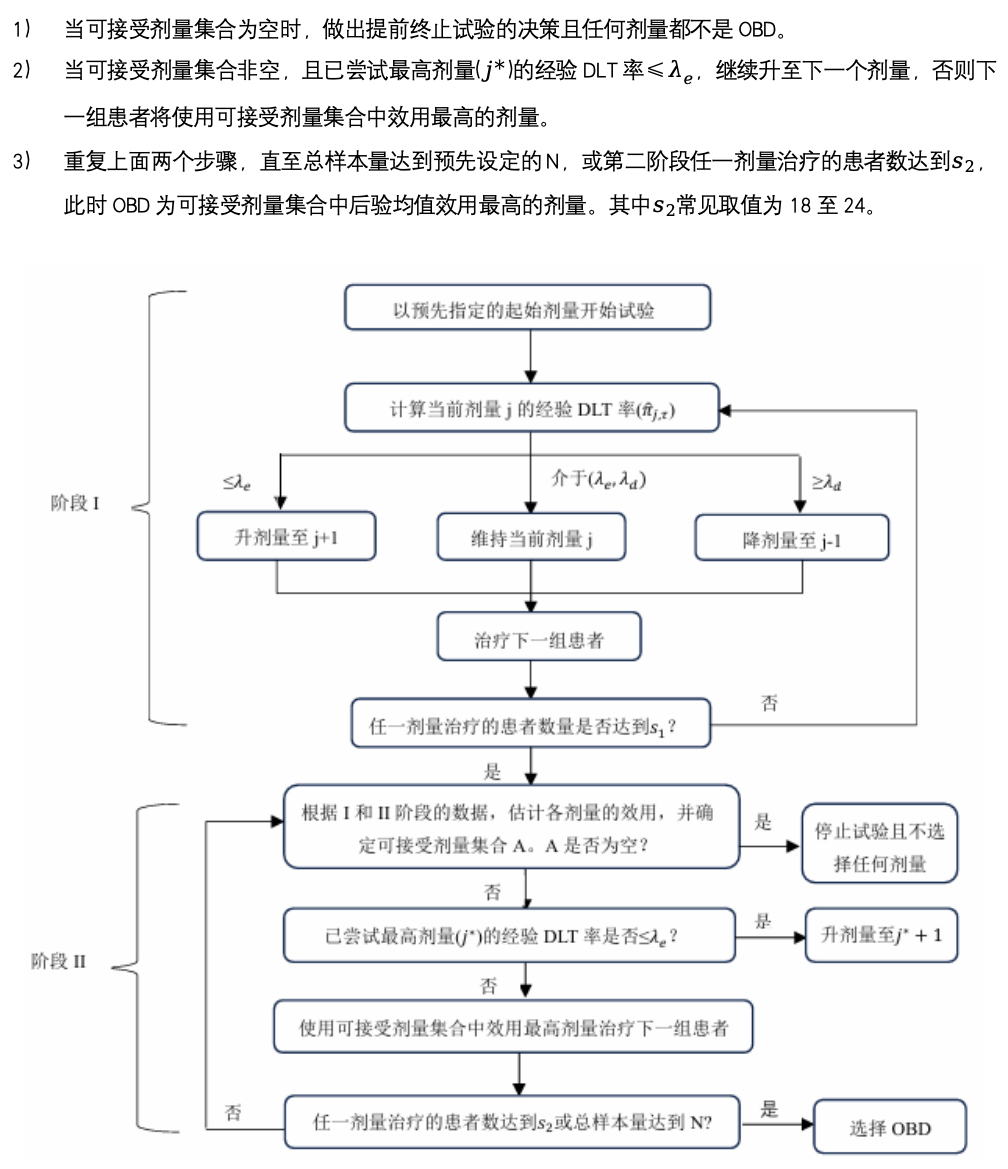
图1:U-BOIN设计流程图
二、U-BOIN执行要点
在实际执行中,可通过Web版http://www.trialdesign.org或http://trialdesign.cn/提供的可视化的应用程序进行U-BOIN设计的实现,无需编写程序,只要根据实际情况填写相应的参数即可快速生成决策表格等,还可以自定义场景进行试验模拟,其界面简洁、操作直观,能够一键生成。
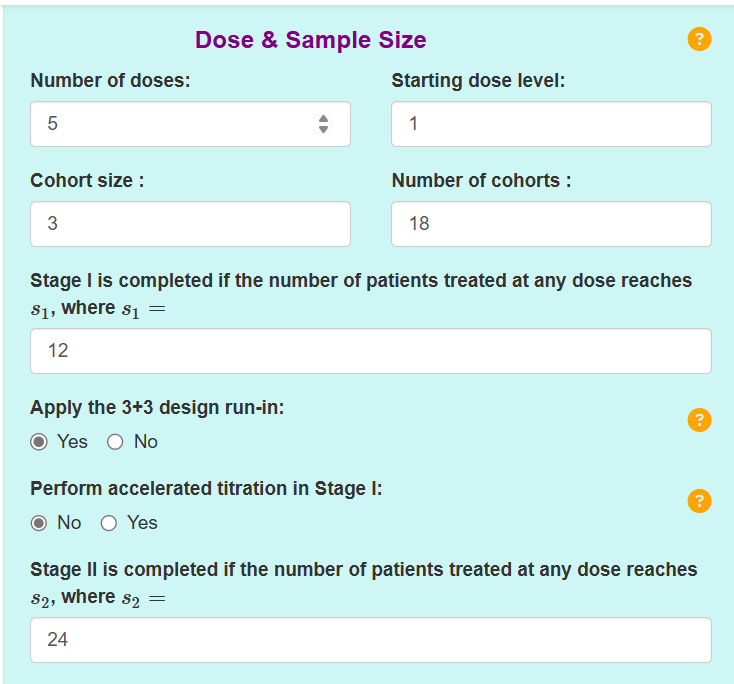
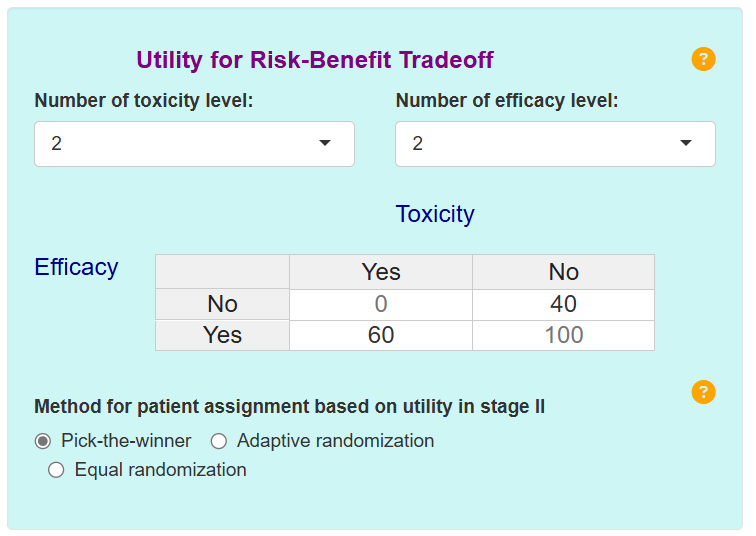

三、总结
U-BOIN设计通过结合多项式-狄利克雷模型、效用函数和动态剂量调整,显著提升了I/II期临床试验中推荐剂量的准确性、灵活性和安全性。其特别适合于毒性和疗效波动大的复杂药物(比如免疫疗法或双通道疗法),同时对传统药物试验也具备良好的适用性。
U-BOIN不仅简化了试验设计的实施,还增强了对复杂临床场景的适应力,彰显了其在现代新药开发中的重要价值。
由Ruitao Lin教授等人提出的BOIN12设计是近年来肿瘤临床试验领域的重要创新,作为BOIN设计在I/II期临床试验中的另一种拓展,它通过单阶段方案实现毒性-有效性的动态权衡,显著提升了剂量探索的效率和准确性。BOIN12设计将在后续文章中进行介绍,敬请关注。
参考文献:
[1] Zhou Y, Lee JJ, Yuan Y. A utility-based Bayesian optimal interval (U-BOIN) phase I/II design to identify the optimal biological dose for targeted and immune therapies. Stat Med. 2019 Dec 10;38(28):5299-5316. doi: 10.1002/sim.8361.
撰写:王素丽
审核:张子豹