2025-12-01
有临来雅
在传统肿瘤临床研究中,I/II期试验通常基于“剂量越高,毒性与疗效越强”的假设,致力于寻找最大耐受剂量(MTD)和后续的II期推荐剂量(RP2D)。然而,随着靶向药物和免疫治疗的发展,这一假设已被打破——剂量增加未必带来疗效提升,反而可能导致疗效趋于平缓,甚至下降。因此,研究者逐渐将目光转向能够在疗效与毒性之间实现最佳平衡的剂量,即最优生物剂量(OBD),而它往往低于MTD。为精准定位OBD,基于效用的模型辅助设计BOIN12应运而生,该设计将临床对疗效与安全性的综合判断量化为“效用”值,通过单阶段自适应流程,结合预生成的基于秩的满意度指数(RDS)决策表,实现无需复杂计算、查表即可智能引导剂量决策。BOIN12正逐步成为新一代免疫与靶向治疗临床试验中不可或缺的剂量优化工具。
BOIN12设计优势如下:
一、BOIN12设计原理
1.毒性-有效性权衡:定义四种结局的效用
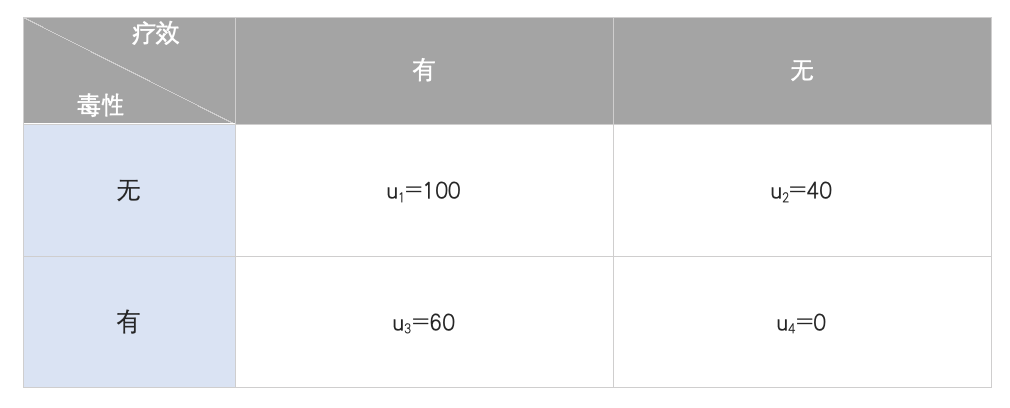
设计的起点,是要求临床医生对药物治疗的四种可能二元结局进行效用值评估。这四种结局构成了决策分析的基本单元,如表1所示:
表1 针对二元疗效与毒性终点的效用表
2. 基于拟二项模型的贝叶斯更新
随着试验数据的积累,BOIN12通过一个创新的拟二项模型来动态学习每个剂量的真实价值。该模型巧妙地利用预设的效用值,将四种离散的临床结局(如“有效且无毒”、“无效但有毒”等)下观察到的患者数据,融合为一个连续的加权得分。
3. 直观的查表决策
在决定为下一组患者分配哪个剂量时,BOIN12不依赖复杂的实时计算,而是采用一个更稳健的标准:评估当前剂量“表现优异”的可能性有多大。为了将这一统计概念落地为临床工具,研究者可以预先获得一份RDS表。在试验过程中,医生只需根据当前剂量下累计的患者数、观察到毒性的人数和有效的人数,像查字典一样在此表中找到对应的满意度指数。指数越高的剂量,代表其越令人满意,从而直接指导下一步的剂量选择。
二、BOIN12执行流程
1.参数设置阶段(图1)
图1 参数设置模拟图


2.剂量探索算法(图2)
BOIN12采用智能剂量探索规则:
1.以最低剂量治疗第一组患者
2.根据当前剂量观察数据:
3.重复第2步直至达到最大样本量
图2 贝叶斯最优区间 I/II 期(BOIN12)设计方案示意图
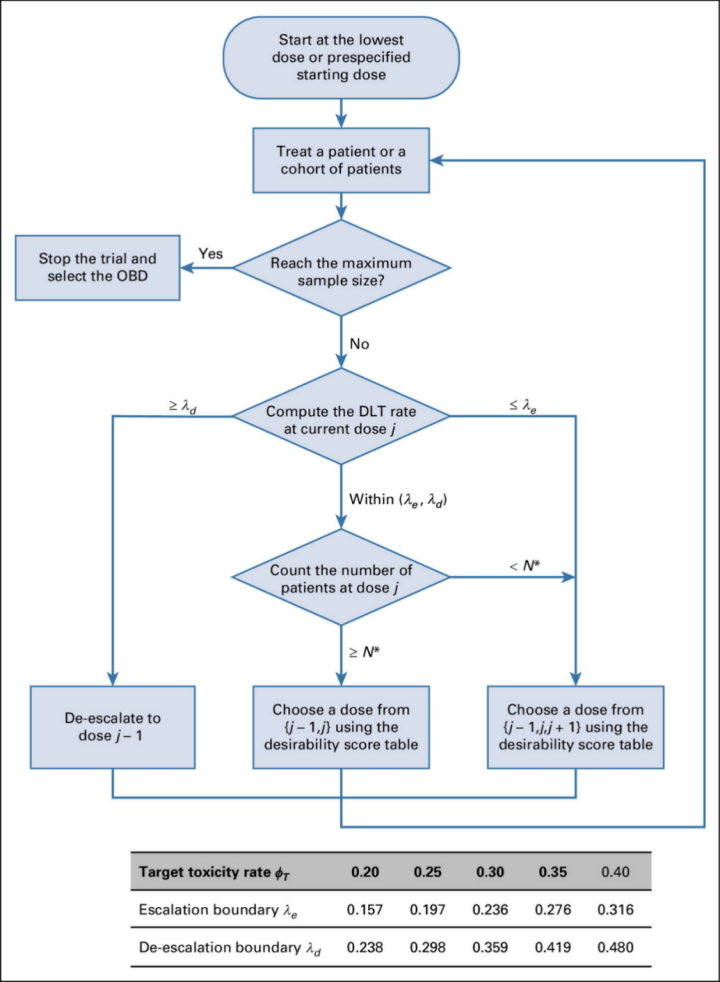
注释:其中(λe,λd)是引自BOIN设计方案的一对优化剂量递增与递减边界,N*为预设样本量截断值(例如N* = 6)。DLT指剂量限制性毒性;OBD指最佳生物剂量。
3.决策表生成
在线工具(https://trialdesign.org/one-page-shell.html#BOIN12)根据输入参数自动生成RDS决策表。表2是u2=40, u3=60时的部分决策表示例:
表2 BOIN12设计的RDS决策表
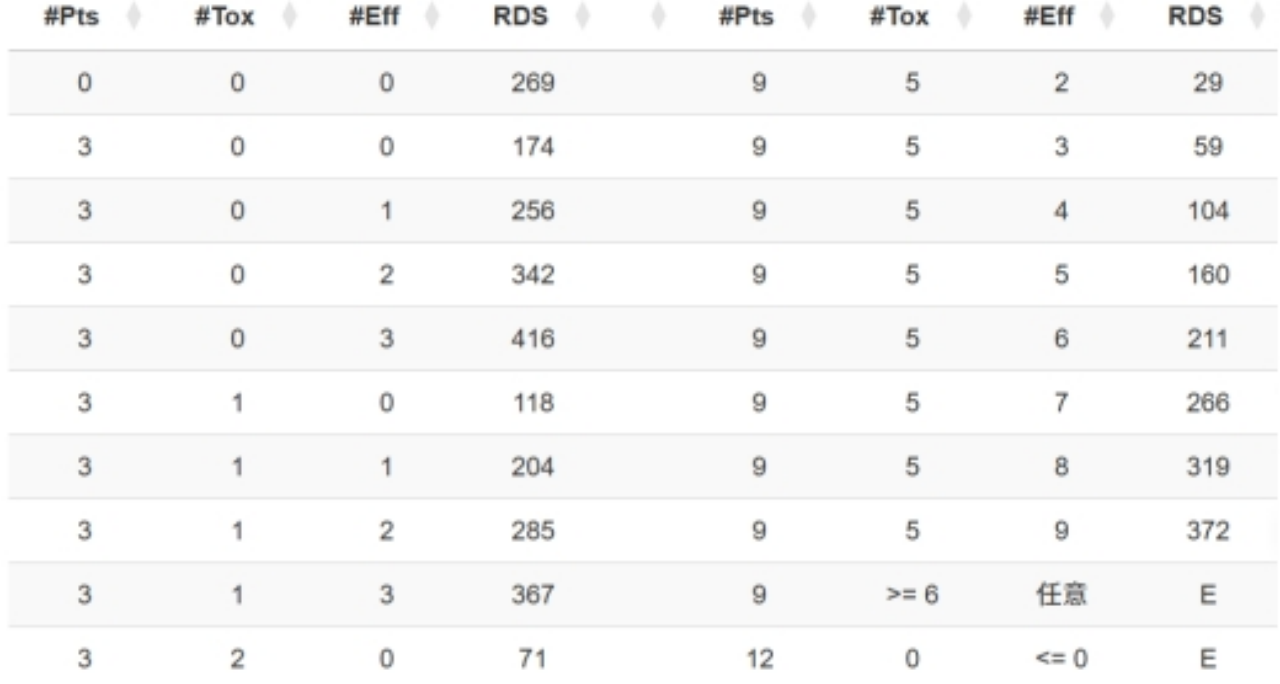
注:#Pts表示当前剂量水平下可评估患者人数;#Tox表示出现毒性的可评估患者人数;#Eff表示出现疗效的可评估患者人数;“E”代表剂量由于过毒或无效而不可接受,应该被剔除。RDS值越大表示剂量越理想,任何RDS值均被视为优于“E”状态。
4.最终剂量选择
当试验达到最大样本量后,进行最终剂量的选择:
三、在线工具使用指南
BOIN12设计可通过以下平台轻松实现:
推荐平台:https://trialdesign.org/one-page-shell.html#BOIN12
四、梳理与比较
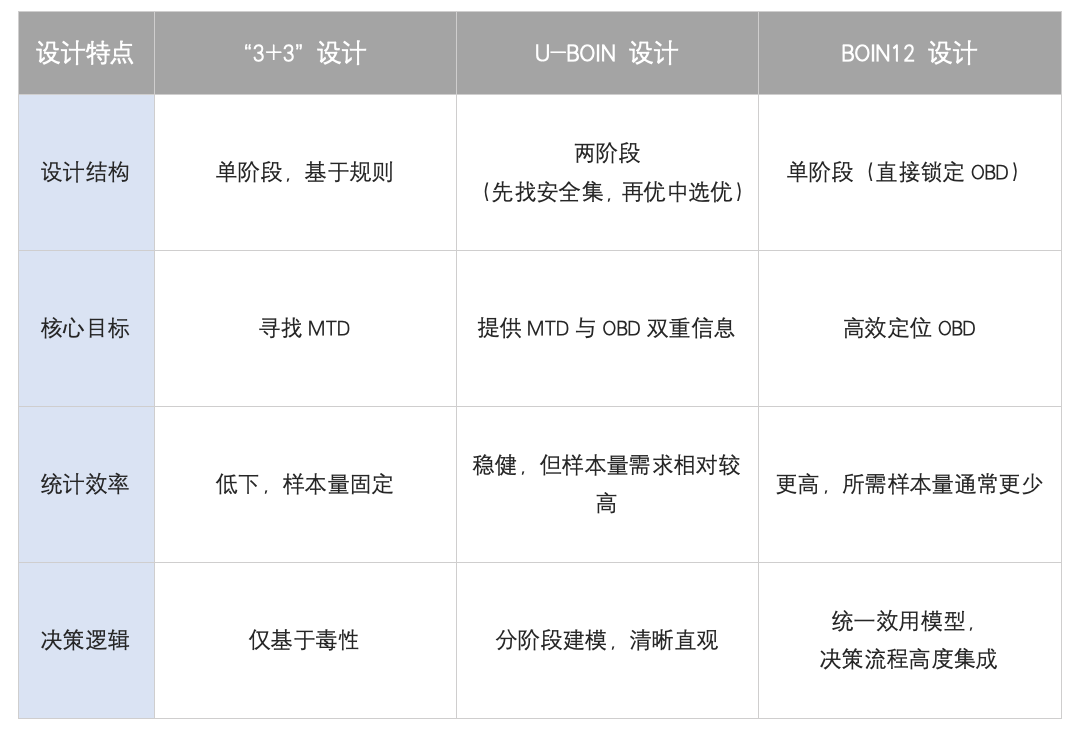
为清晰对比不同剂量探索设计的特点,将“3+3”设计、U-BOIN设计与BOIN12设计在设计结构、核心目标、统计效率及决策逻辑等维度进行了梳理与比较,详见表3。
表3 试验设计比较表
五、总结
BOIN与BOIN12设计均将BOIN设计拓展至I/II期临床试验,采用效用函数进行自适应剂量寻找,核心目标均为确定OBD。
两者主要区别在于:U-BOIN采用两阶段设计,先基于毒性筛选出安全有效的剂量集合,再从中优化选择OBD,其优势在于流程清晰、易于解释,并可同时提供MTD与OBD双重信息;而BOIN12采用单阶段设计,直接基于加权效用的贝塔-二项模型进行剂量优化,整体围绕OBD展开,具有更高的统计效率,通常所需样本量更少。
因此,若临床试验重视MTD与OBD的双重输出且需易于沟通,可选用U-BOIN;若主要目标为高效定位OBD并节省样本量,则BOIN12更为适合。两者均为模型辅助设计,兼具稳健性、优良性能与操作简便性。
撰写:王晶宇
审核:王素丽、李纪杰