2026-03-26
有临来雅

在之前的文章中,我们探讨了BF-BOIN如何在I期试验中“既快又准”,也解读了U-BOIN如何引入“效用函数”开启靶向药研发新范式。U-BOIN凭借其两阶段设计的稳健性,赢得了众多研究者的青睐。
然而,面对样本量极度紧缺的罕见肿瘤试验,或是机制明确的靶向药物研发,是否有更极致的效率方案?本期,我们将深入解读BOIN家族的另一位成员——BOIN-12设计。它摒弃了分阶段策略,以单阶段流程直取OBD,正在引领一场剂量优化的“效率革命”。
一、 核心演进:从“稳扎稳打”到“单刀直入”
BOIN-12与U-BOIN虽然核心目标一致——均为精准定位最优生物剂量(OBD),但路径选择截然不同。
【互动投票】在您的早期临床试验中,更倾向于哪种策略?
A. U-BOIN:稳扎稳打,兼顾MTD与OBD,便于监管沟通。
B. BOIN-12:目标明确,追求样本量最小化与效率最大化。
C. 视情况而定:需根据药物机制(如细胞毒 vs 靶向免疫)具体分析。

(欢迎扫码参与互动投票,我们将抽取3位幸运读者送出精美小礼品!)
二、 深度解析:BOIN-12的三大技术支柱
BOIN-12之所以能实现高效决策,依赖于三个关键环节的精密配合。
1. 量化临床直觉:效用函数的科学设定
设计的起点是将医生的临床判断“数字化”。BOIN-12要求针对四种二元结局设定效用值(u1-u4),这不仅仅是打分,更是对治疗目标的界定。
2. 算法内核:准贝塔-二项模型与RDS指数
准贝塔-二项模型是BOIN-12的“大脑”,它将离散的四种结局数据,融合为连续的加权得分,并最终转化为基于秩的满意度指数(RDS)。
RDS表是BOIN-12“免计算”的关键。它预先生成了所有可能的临床情境(患者数、毒性数、有效数),并在后台完成了复杂的贝叶斯后验概率计算。试验中,研究者只需查表,即可知道当前剂量“表现优异”的概率。
3. 关键决策逻辑:探索与优化的平衡
BOIN-12的算法不仅仅是简单的“升剂量”或“降剂量”,其核心逻辑包含一个重要的截断机制:
三、 实战落地:如何避免决策陷阱?
在实际操作中,有两个细节需要特别注意,以确保试验的科学性:
1.“可接受”是决策的前提
在查阅RDS表进行剂量比较前,必须先通过“可接受性”测试。若某剂量毒性率过高(如超过预设上限φT)或疗效率过低(低于预设下限φE),该剂量将被标记为“E”(Eliminate),直接剔除,不参与RDS比较。任何RDS值均优于“E”状态,这体现了“安全/有效底线优先”的原则。
2.工具辅助与方案生成
复杂的建模过程已由在线工具(https://trialdesign.org/one-page-shell.html#BOIN12)完成。研究者只需输入参数(φT , φE, u2, u3等),系统即可自动生成:
四、总结:如何做出最终选择?
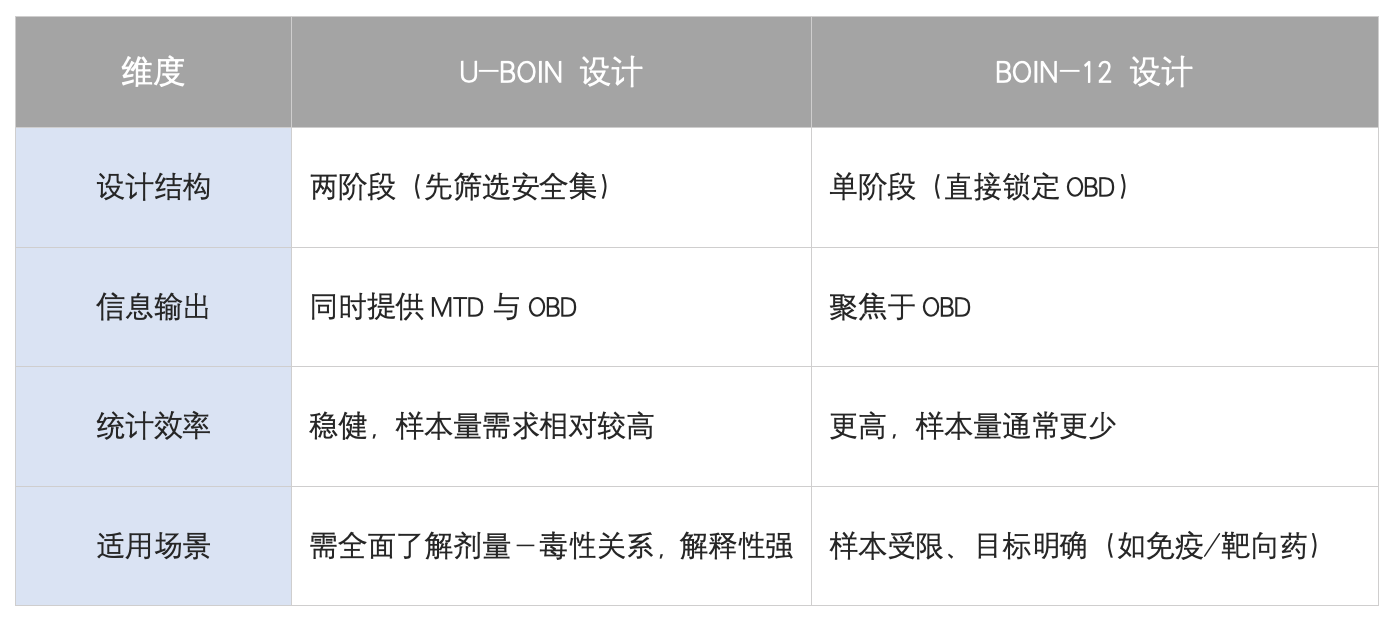
您在临床试验设计中遇到过哪些“两难”抉择?欢迎在评论区分享您的经验!
【参考文献】
[1] Yuan Y, Lee JJ, Hilsenbeck SG. BOIN12: Bayesian Optimal Interval Phase I/II Trial Design for Dose Optimization in Oncology. *Clinical Cancer Research*. 2019;25(14):4624-4633.
[2] Zhou H, Murray TA, Pan H, Yuan Y. Comparative review of novel model-assisted designs for phase I/II clinical trials in oncology. *Contemporary Clinical Trials*. 2022;119:106835.
[3] Lin R, Yuan Y. Time-to-event Bayesian optimal interval phase I/II trial design for dose optimization. *Biometrics*. 2020;76(4):1157-1166.