2025-10-14
有临来雅

Simon两阶段设计是Ⅱ期肿瘤临床试验中较为常用的设计。该设计将整个试验分为两个阶段,在第一阶段末将观察到的应答人数与预先设定的试验停止边界进行比较,一旦发现试验药无效,则立即停止试验;反之则进入第二阶段,继续验证试验药的有效性。该设计的优点是能在控制Ⅰ类错误以及Ⅱ类错误的前提下,使试验药无效时平均入组患者人数达到最小。
一、Simon两阶段设计简介
Simon两阶段设计基于假设检验框架评价试验药的有效性。令p代表试验药的真实反应率,该设计原假设为H0: p ≤ p0,备择假设为H1: p ≥ p1,其中p0代表过低的反应率,p1代表期望达到的最低反应率。即原假设表示该试验药的应答率过低而不值得进一步研发;而备择假设认为试验药有效率已达到预期要求因此值得进一步研发。
Simon两阶段设计可描述如下,在试验第一阶段,入组n1例可评估患者,并假设其中r1*例患者出现有效性反应。若r1*≤r1(其中r1为第一阶段停止边界,一般是一个较小的值),则接受H0,认为药物无效,此时出于伦理考虑,应停止试验;反之,若r1*>r1,则进入第二阶段继续入组n2例可评估患者,并假设在所有n1+n2例接受治疗的患者中共有r*例患者出现有效性反应。若r*≤r(r是所有受试者中出现有效反应的例数边界),则接受H0,认为试验药无效;反之,若r*>r,则拒绝H0,认为试验药有效。在该设计中需要设定的未知设计参数为(n1,r1,n2,r)。上述参数可通过控制Ⅰ类错误及Ⅱ类错误,最小化当H0为真时平均入组患者数来确定。
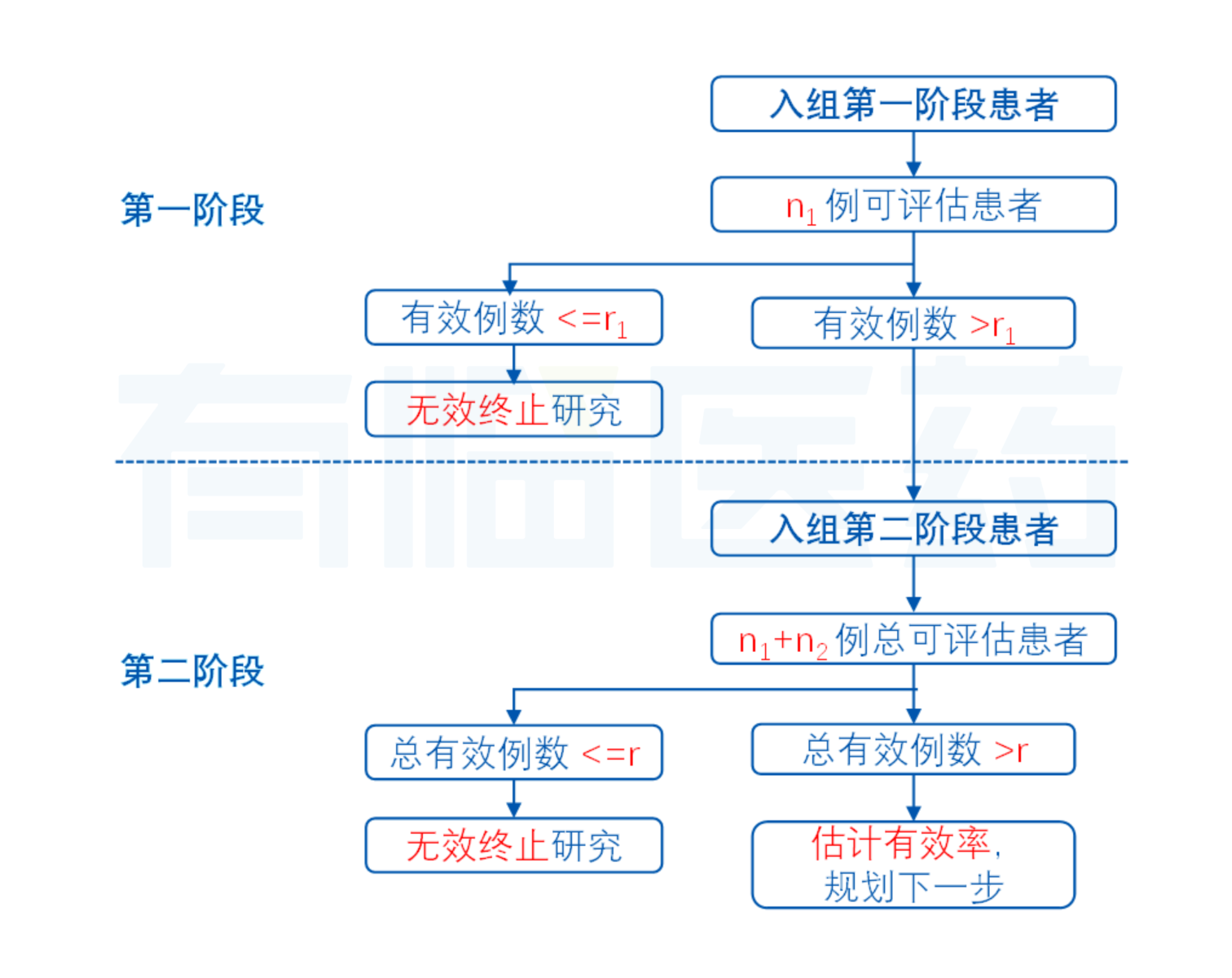
图1 Simon两阶段设计示意图
二、Simon两阶段的设计
在控制Ⅰ类错误率α和Ⅱ类错误率β的前提下,可通过枚举的方法确定试验设计的参数值:
Optimal:在H0为真时(即试验药实际无效)最小化样本量N的期望值E(N/H0)。
Minimax:最小化试验的实际最大样本量n = n1+n2
Adaptive:提供更灵活的期中分析和决策选项,不局限于一次期中分析。
Admissible:在给定的设计类别中,确保所选的设计方案在所有重要的比较标准下,都不存在另一个严格优于它的设计。
样本量计算工具:PASS软件、R软件或www.trialdesign.cn网站
三、Simon两阶段适用场景及注意事项
1.适用场景
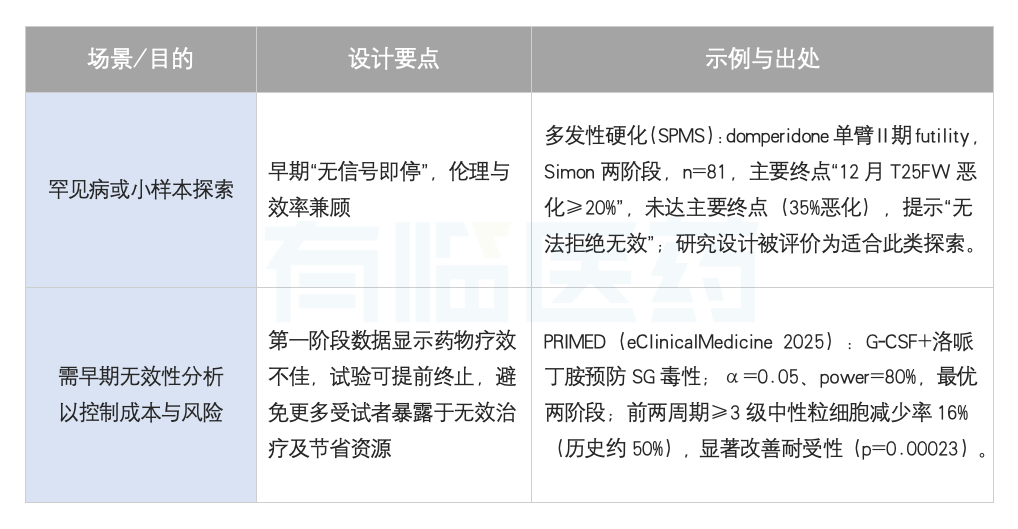
2.实际案例
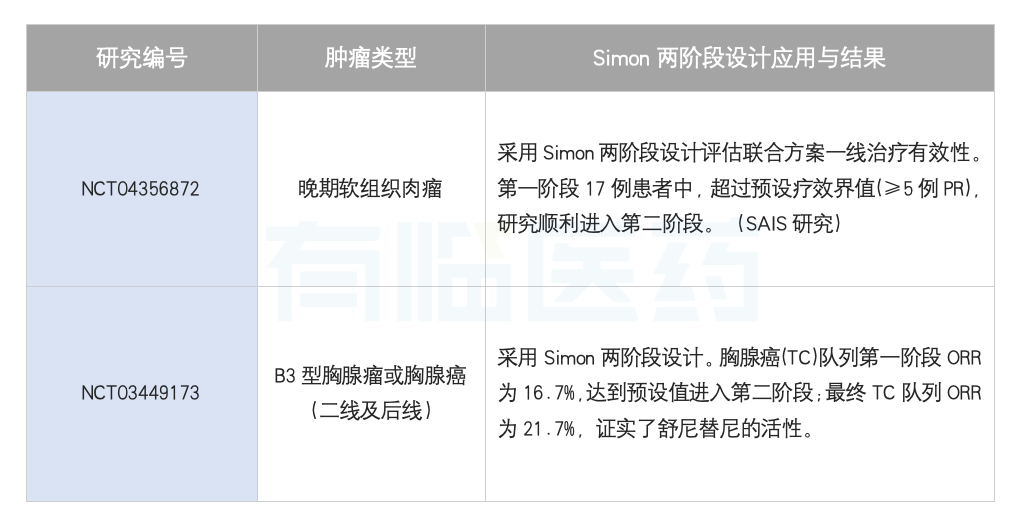
3.注意事项
第一,Simon两阶段只适用有效性终点为二分类结局的研究。
第二,Simon两阶段需预先设定“无效”率和“期望有效”率。
第三,Simon两阶段设计是基于频率论的,无法利用历史数据和先验信息以提高试验的功效和成功率。
四、Simon两阶段的软件实现方法
1.R包clinfun使用说明(R实现)
【R包clinfun使用说明】
计算Richard Simon给出的Optimal和Minimax Phase Ⅱ设计用法:
ph2simon(p0, p1, α, β, nmax = 100)
参数说明:
【p0】:现有对照药预估的有效率
【p1】:试验药符合临床预期的有效率
【α】:Ⅰ类错误
【β】:Ⅱ类错误
【nmax】:最大总样本量(默认为100;最多为500)代码
五、实例分析(R&trialdesign&PASS)
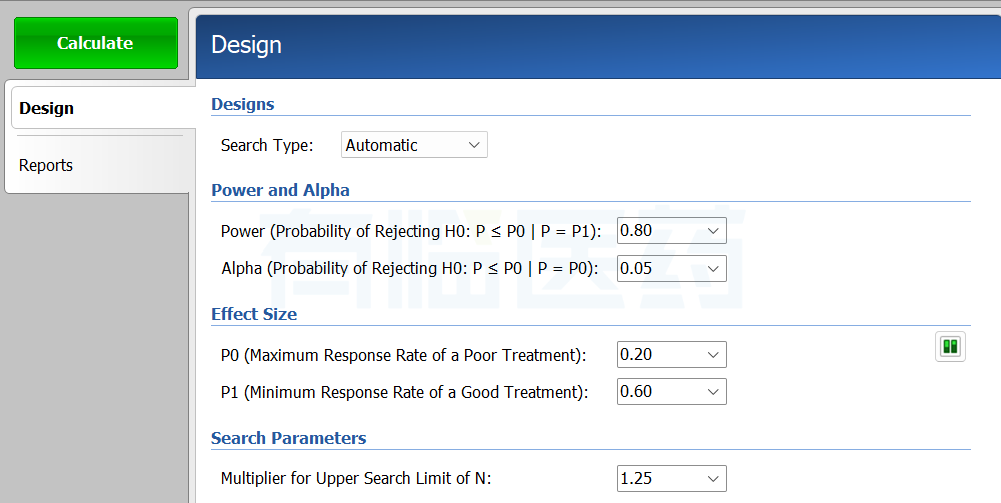
假如有一种新的试验药物与已知有效的对照药物进行Ⅱ期对照试验,预计新药的有效率为p1=60%,对照药物的有效率p0=20%,取α=0.05,1-β=80%。
1.R代码
#载入R包
library(clinfun)
#现有对照药预估的有效率
p0<-0.2
#试验药符合临床预期的有效率
p1<-0.6
#I类错误(单侧)
α <-0.05
#II类错误
β <-0.2
#输入函数
ph2simon(p0,p1, α, β , nmax=100)
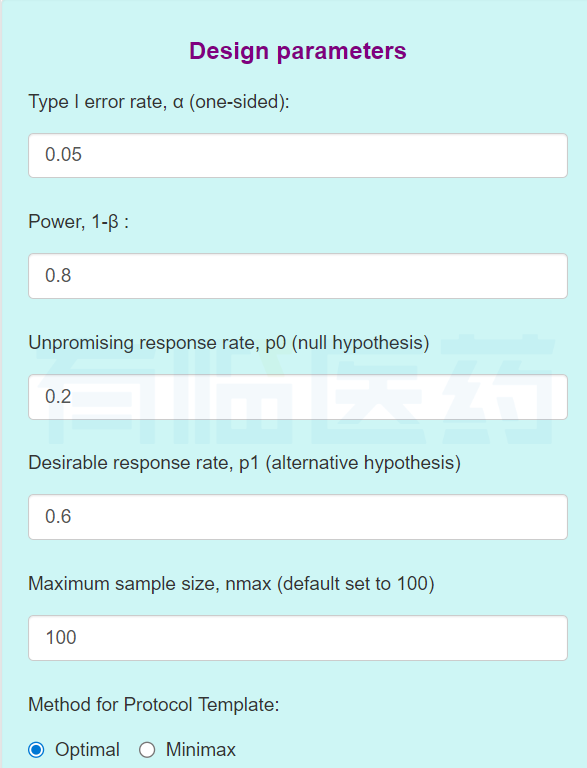
2.trialdesign网站
3.PASS
4.计算结果

图2 R运行结果
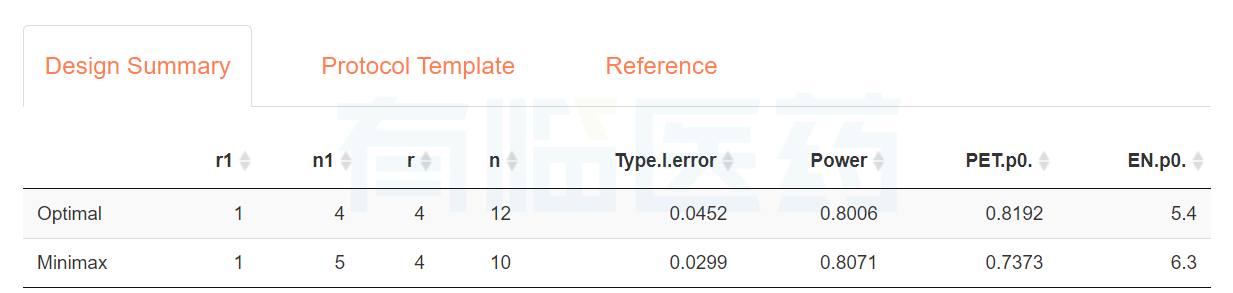
图3 trialdesign运行结果
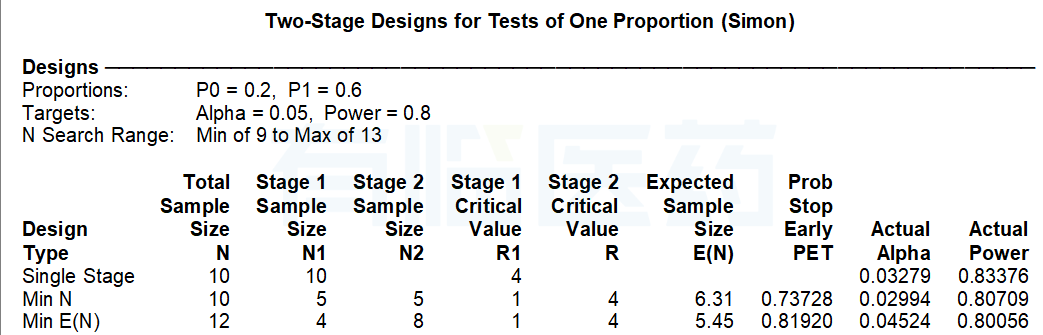
图4 PASS运行结果
5.结果解读
如图2、图3和图4可知两种方法的计算结果一致,当最优化设计时,在第一阶段选择4例患者进入试验,若观察到的有效例数不超过1则终止试验,认为药物没有研发前景;否则进入第二阶段,并增加总患者例数到12,此时如果有效例数不超过4个则终止试验,否则认为药物有效。当极小极大设计时,第一阶段选择5个患者进入试验,若观察到的有效例数不超过1则终止试验;否则进入第二阶段,并增加总患者例数到10例,此时如果有效病例数不超过4则终止试验,否则认为药物有效。
六、总结
Simon两阶段设计常用于肿瘤药物的单臂两阶段试验,该设计能够节省样本量,并更早终止无效治疗的试验,从而避免受试者接受无效治疗。同时,它使治疗效果的统计评估更贴合研究的治疗目标。在实施过程中,研究者可根据研发策略选择极小极大或最优化设计以确定样本量,统计师也可根据不同情况调整第二阶段的入组人数,从而真正为病人谋取福利。
注:更多Simon设计即将更新,敬请期待。
参考文献
[1] 言方荣,王骏,袁鹰.肿瘤临床试验贝叶斯设计方法[M].北京:人民卫生出版社,2021.
[2]Simon R. Optimal two-stage designs for phase II clinical trials. Control Clin Trials. 1989 Mar;10(1):1-10. doi: 10.1016/0197-2456(89)90015-9. PMID: 2702835.
[3]Phase II Clinical Trials in Oncology: Strengths and Limitations of Two-Stage Designs Optimal Two-Stage Designs for Phase II Clinical Trials.
撰写:黄美琪
审核:李纪杰